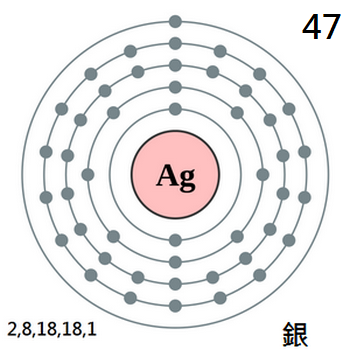
 銀是一種化學元素,化學符號Ag(來自拉丁語Argentum),
銀是一種化學元素,化學符號Ag(來自拉丁語Argentum),
銀(化學元素)
 銀是一種化學元素,化學符號Ag(來自拉丁語Argentum),
銀是一種化學元素,化學符號Ag(來自拉丁語Argentum),
原子序數47,是一種銀白色的過渡金屬。
銀在自然界中很少量以游離態單質存在,
主要以含銀化合物礦石存在。
銀的化學性質穩定,活躍性低,價格貴,導熱、導電性能很好,
不易受化學藥品腐蝕,質軟,富延展性。
其反光率極高,可達99%以上。
銀字屬於艮字族。在艮字族裡,艮字都是聲符兼義符。
艮字族漢字都與“邊界”、“極限”之義有關。
銀的本義是“(價值)接近于黃金的金屬”。
純銀是一種美麗的銀白色的金屬,它具有很好的延展性,
其導電性和傳熱性在所有的金屬中都是最高的。
銀是古代發現的金屬之一。銀在自然界中有單質存在,但絕大部分是以化合態的形式存在。
銀具有很高的延展性,因此可以碾壓成只有0.00003釐米厚的透明箔,1克重的銀粒就可以拉成約兩公里長的細絲。
銀的導熱性和導電性在金屬中名列前茅。


理化性質
同位素
平常見到的銀是銀107和銀109,其中銀107的豐度最多(51.839%)。
銀的同位素的豐度幾乎相同,這在元素週期表中十分罕見。銀的原子量是107.8682(2) 克/摩爾。
化學家已經研究了銀的二十八個放射性同位素的特性,最穩定的為Ag(半衰期為41.29日),
第二穩定的為Ag(半衰期為7.45日),第三穩定的為Ag(半衰期為3.13小時)。
銀有很多亞穩定同位素,最穩定的為Ag(半衰期為418年),
第二為Ag(半衰期為249.79日),第三為Ag(半衰期為8.28日)。
其餘的放射性同位素的半衰期皆小於一小時,大部分同位素的半衰期皆小於三分鐘。
銀的同位素的原子量最少為92.950(銀93),最多為129.950(銀130)。
鈀107和鎘107的衰變產物是銀107,豐度最多的穩定同位素。
鈀107的衰變模式是貝塔衰變,鎘107的衰變模式是電子捕獲。
Pdβ衰變成Ag的半衰期為650萬年。鐵隕石是唯一含有可供測量Ag富度變化的足量的“鈀-銀比”。
放射性的銀在1978年在美國的聖塔克拉拉被發現。
它的發現者提出,一些小型鐵核的行星(如地球)與其異體,可能是在一千多萬年前的核合成事件中產生的。
從這熔化過的星球本體中,觀察到的Pd–Ag比值,反映出早期太陽系的吸積中應存在著不穩定的核種。


化學性質
銀溶于硝酸,生成硝酸銀。硝酸銀是一種透明晶體,有感光性,且易溶于水。
硝酸銀是合成許多其他銀化合物的原料,也可作為防腐劑,還用於彩色玻璃中的黃色添加劑。
銀不易與硫酸反應,因此硫酸在珠寶製造中用於清洗銀焊及退火後留下的氧化銅火痕。
銀易與硫以及硫化氫(H2S)反應生成黑色的硫化銀(Ag2S),這在失去光澤的銀幣或其他物品上很常見,
銀在高溫下也可以和氧氣反應,生成棕色的氧化銀(Ag2O)
。當銀制電氣觸點在富含硫化氫的環境下工作時,觸點上的硫化銀還會生成銀晶須。
與硫化氫和氧氣反應:4Ag +2 H2S + O2 = 2Ag2S + 2H2O
與濃硫酸反應: 2Ag + 2H2SO4(濃) ====
Ag2SO4 + SO2↑ + 2H2O
與鹵族元素反應:
2Ag + F2 ===== 2AgF
暗棕色
2Ag + Cl2 ===== 2AgCl
白色
2Ag + Br2 ===== 2AgBr
淡黃色
2Ag + I2 ===== 2AgI
黃色
與硫反應:2Ag + S ==== Ag2S
與氧氣反應:4Ag + O2 ==== 2Ag2O
向硝酸銀溶液中加入氯離子會沉澱出氯化銀(AgCl),
同樣地,加入溴鹽或碘鹽可以沉澱出用於製造感光乳劑的其他鹵化銀。
氯化銀用於製造檢測pH值和測量電位的玻璃電極,以及用於玻璃的透明水泥。
將碘化銀 (AgI)撒入雲層以人工降雨。鹵化銀在水溶液中高度不溶(除了氟化銀),因而常用於重量分析。
向硝酸銀溶液加入堿,沉澱得到氧化銀 (Ag2O)。
氧化銀用作紐扣電池的正極。向硝酸銀溶液加入碳酸鈉 (Na2CO3),沉澱得碳酸銀(Ag2CO3)。
2 AgNO3 + 2 OH-
→ Ag2O + H2O + 2 NO3 -
2 AgNO3 + Na2CO3
→ Ag2CO3 + 2 NaNO3
雷酸銀(AgONC)是一種強烈的、對碰撞敏感的炸藥,是銀與硝酸在乙醇(C2H5OH)的存在下反應得到的,用於雷管。
其他危險易爆的銀化合物包括疊氮化銀 (AgN3),由硝酸銀與疊氮化鈉 (NaN3)反應得到,
還有乙炔銀(Ag2C2),由硝酸銀或銀氨溶液與乙炔(C2H2)反應得到。
鹵化銀晶體曝光後形成的潛像經還原劑,
如氫醌、米吐爾(4-(甲氨基)苯酚硫酸氫鹽)或抗壞血酸的鹼性溶液顯影處理後,曝光的鹵化銀被還原成金屬銀。
硝酸銀的鹼性溶液(銀氨溶液)可被還原糖,如葡萄糖等還原為金屬銀,這個反應用於製造銀鏡,以及玻璃聖誕飾品的內表面。
鹵化銀可溶於硫代硫酸鈉(Na2S2O3)溶液,因此硫代硫酸鈉可作為定影劑,去除顯影後感光乳劑上多餘的鹵化銀。
在溴化鉀(KBr)的存在下,金屬銀可被強氧化劑如高錳酸鉀(KMnO4)或重鉻酸鉀(K2Cr2O7)侵蝕;
這些化合物在攝影中用於漂白可見影像,將其轉化為鹵化銀,既可以被硫代硫酸鈉去除,
又可以重新顯影以加強原始的影像。
在過量的氰根離子(CN)存在下,氰化銀(AgCN)可以形成可溶于水的氰配合物(Ag(CN)2)。
銀的氰配合物溶液用於電鍍銀。
製備方法
從自然界提取的銀有的是游離態,有的是化合物。
游離態的銀可直接清洗後除雜成品。銀的化合物可在隔絕空氣下高溫加熱,再用一氧化碳還原即可。
 發現歷史
發現歷史
在古代,人類就對銀有了認識。
銀和黃金一樣,是一種應用歷史悠久的貴金屬,
至今已有4000多年的歷史。
由於銀獨有的優良特性,人們曾賦予它貨幣和裝飾雙重價值,
英鎊和我國解放前用的銀元,就是以銀為主的銀、銅合金。
銀白色,光澤柔和明亮,是少數民族、佛教和伊斯蘭教徒們喜愛的裝飾品。
銀首飾亦是全國各族人民贈送給初生嬰兒的首選禮物。
歐美人士在復古思潮影響下,佩戴著易氧化變黑的白銀鑲淺藍色綠松石首飾,給人帶來對古代文明無限美好的遐思。
而在國內,純銀首飾亦逐漸成為現代時尚女性的至愛選擇。
銀是古代就已經知道的金屬之一。
銀比金活潑,雖然它在地殼中的豐度大約是黃金的15倍,但它很少以單質狀態存在,因而它的發現要比金晚。
在古代,人們就已經知道開採銀礦,由於當時人們取得的銀的量很小,使得它的價值比金還貴。
西元前1780至 1580年間,埃及王朝的法典規定,銀的價值為金的2倍,
甚至到了17世紀,日本金、銀的價值還是相等的。
銀最早用來做裝飾品和餐具,後來才作為貨幣。
 純銀是一種美麗的白色金屬,
純銀是一種美麗的白色金屬,
銀的化學符號Ag,來自它的拉丁文名稱Argentum,
是“淺色、明亮”的意思。
它的英文名稱是Silver。月亮般的金屬——銀
銀,永遠閃耀著月亮般的光輝,
銀的論文原意,也就是“明亮”的意思。
我國也常用銀字來形容白而有光澤的東西,
如銀河、銀杏、銀魚、銀耳、銀幕等。
我國古代常把銀與金、銅並列,稱為“唯金三品”。
《禹貢》一書便記載著“唯金三品”,
可見我國早在西元前二十三世紀,即距今四千多年前便發現了銀。
在大自然中,人們曾找到一塊重達13.5噸的純銀!另外,也有以氯化物與硫化物的形式存在,
常同鉛、銅、銻、砷等礦石共生在一起。
銀在自然界中較少以單質狀態存在,大部分是化合物狀態,因而它的發現要比金晚,一般認為在距今5500-6000年以前。
天然銀多半是和金、汞、銻、銅或鉑成合金,天然金幾乎總是與少量銀成合金。
我國古代已知的琥珀金,在英文中稱為ELECTRUM,就是一種天然的金、銀合金,含銀約20%。
最初由於人們取得銀的量很小,使得它的價值比金還貴。
在大約西元前1780-1580年間埃及王朝的法典中規定,銀的價值是金的兩倍。
甚至到17世紀,在日本銀和金的價值還是相等的。馬克思在《政治經濟學批判》中講到:
“……而銀的開採卻以礦山勞動和一般比較高度的技術發展為前提。
因此,雖然銀不那麼絕對稀少,但是它最初的價值卻相對地大於金的價值。”
人類發現和使用銀的歷史至少已有兩千年了。
我國考古學者從出土的春秋時代的青銅器當中就發現鑲嵌在器具表面的“金銀錯”(一種用金、銀絲鑲嵌的圖案)。
從漢代古墓中出土的銀器已經十分精美。在古代,銀的最大用處是充當商品交換的媒介──貨幣。銀有很強的殺菌能力。
西元前三百多年,馬其頓王國皇帝亞歷山大帶領軍隊東征時,受到熱帶痢疾的感染,大多數士兵得病死亡,東征被迫終止。
但是,皇帝和軍官們卻很少染疾。
這個迷直到現代才被解開。
原來皇帝和軍官們的餐具都是用銀製造的,而士兵的餐具都是用錫製造的。
銀在水中能分解出極微量的銀離子,這種銀離子能吸附水中的微生物,使微生物賴以呼吸的酶失去作用,從而殺死微生物。
銀離子的殺菌能力十分驚人,十億分之幾毫克的銀就能淨化1千克水。
我國古代法醫早就懂得用"銀針驗屍法"來測定死者是否中毒而死,幫助破獲了不少謀殺案件。
銀還是一種可為人類食用的金屬,在我國和印度均有用銀箔包裹食品和丸藥服用的記載。
同時銀還是某些生物的食物。據我國古籍《天香樓外史》記載:
古時候有一個婦人藏了150兩私房銀。有一天她開箱查看藏銀,銀竟不翼而飛。
婦人大吃一驚,懷疑被人盜走,一時弄得全家人心惶惶。
後來再開箱尋找,只見一大堆白蟻正團團集在一起,吃著殘存的銀粒。
婦人一氣之下,把白蟻投入爐中,以解心頭之恨。“火燒蟻死,白銀複出”,一稱,恰好150兩。
礦產分佈
中國是銀礦資源中等豐度的國家。
銀礦主要有輝銀礦,其次是角銀礦,也有自然銀。
由銀礦與食鹽和水共熱,再與汞結合為銀汞齊,蒸去汞而得銀。或由銀礦以氰化堿類浸出後加鉛或鋅使銀沉澱而制得。
工業應用
電子電器是用銀量最大的行業,其使用分為電接觸材料、複合材料和焊接材料。
銀和銀基電接觸材料可以分為:純 Ag類、銀合金類、銀-氧化物類、燒結合金類。
全世界銀和銀基電接觸材料年產量約2900~3000t。
複合材料是利用複合技術製備的材料,分為銀合金複合材料和銀基複合材料。
從節銀技術來看,銀複合材料是一類大有發展前途的新材料。銀的焊接材料如純銀焊料、銀—銅焊料等。
感光材料
鹵化銀感光材料是用銀量最大的領域之一。
目前生產和銷售量最大的幾種感光材料是攝影膠捲、相紙、X-光膠片、螢光資訊記錄片、電子顯微鏡照相軟片和印刷膠片等。
上世紀90年代,世界照相業用銀量大約在6000~6500t。
由於電子成像、數位化成像技術的發展,使鹵化銀感光材料用量有所減少,
但鹵化銀感光材料的應用在某些方面尚不可替代,仍有很大的市場空間。
化學化工材料
銀在這方面有兩個主要的應用,一是銀催化劑,
如廣泛用於氧化還原和聚合反應,用於處理含硫化物的工業廢氣等。
二是電子電鍍工業製劑,如銀漿、氰化銀鉀等。
工藝飾品
銀具有誘人的白色光澤,較高的化學穩定性和收藏觀賞價值,深受人們(特別是婦女)的青睞,
因此有女人的金屬之美稱,廣泛用作首飾、裝飾品、銀器、餐具、敬賀禮品、獎章和紀念幣。
銀首飾在發展中國家有廣闊的市場,銀餐具備受家庭歡迎。
銀質紀念幣設計精美,發行量少,具有保值增值功能,深受錢幣收藏家和錢幣投資者的青眯。
20世紀90年代僅造幣用銀每年就保持在1000~1500t上下,占銀的消費量5%左右。
 純銀應用
純銀應用
純銀是一種美麗的銀白色的金屬,
它具有很好的延展性,其導電性和傳熱性在所有的金屬中都是最高的。
銀常用來製作靈敏度極高的物理儀器元件,
各種自動化裝置、火箭、潛水艇、電腦、核裝置以及通訊系統,
所有這些設備中的大量的接觸點都是用銀製作的。
在使用期間,每個接觸點要工作上百萬次,
必須耐磨且性能可靠,能承受嚴格的工作要求,銀完全能滿足種種要求。
如果在銀中加入稀土元素,性能就更加優良。
用這種加稀土元素的銀製作的接觸點,壽命可以延長好幾倍。
銀的最重要的化合物是硝酸銀。
在醫療上,常用硝酸銀的水溶液作眼藥水,因為銀離子能強烈地殺死病菌。
生物體中作用
銀的離子以及化合物對某些細菌、病毒、藻類以及真菌顯現出毒性,但對人體卻幾乎是完全無害的。
銀的這種殺菌效應使得它在活體外就能夠將生物殺死。
然而,銀製品的測試以及標準化卻存在很大難度。
希波克拉底曾經有描述銀在治療和防止疾病方面的功用。
腓尼基人曾經用銀制瓶子來盛放水、酒和醋,以此防止這些液體腐敗。
20世紀初期,人們也曾把銀幣放在牛奶裡,以此來延長牛奶的保鮮期。
銀的殺菌機制長期以來一直為人們所爭論探討,但至此還沒有確鑿的定論。
其中一個很好的例子是微動力效應,它成功的解釋了銀離子對微生物的作用,但卻不能解釋其對病毒的作用。
銀大量的添加於凝膠以及繃帶中。銀的抗菌性來源於銀離子。
由於銀離子可以和一些微生物用於呼吸的物質(比如一些含有氧、硫、氮元素的分子)形成強烈的結合鍵,
以此使得這些物質不能為微生物所利用,從而使得微生物窒息而亡。
在抗生素發明之前,銀的相關化合物曾在第一次世界大戰時用於防止感染。
銀作為效用廣泛的抗菌劑正在進行新的應用。
其中一方面就是將硝酸銀溶於海藻酸鹽中,用於防止傷口的感染,尤其是燒傷傷口的感染。
2007年,一個公司設計出一種表面鍍上銀的玻璃杯,這種杯子號稱具有良好的抗菌性。
除此之外,美國食品和藥品管理協會(FDA)也審批通過了一種內層鍍銀的導氣管的應用,
因為研究表明這種導氣管能夠有效的降低導氣管型肺炎。
銀並不會對人的身體產生毒性,但長期接觸銀金屬和無毒銀化合物也會引致銀質沉著症。
因為身體色素產生變化,皮膚表面會顯出灰藍色。雖無毒性,但仍會影響外觀。
銀針試毒的原理
在古代的毒藥大多是砒霜(三氧化二砷),然而在古代的化學技術不發達,
砒霜中會混有大量的硫或硫化物(約10%)。銀會與硫反應生成硫化銀黑色沉澱,從而試毒。