 歷史
歷史
鋦
 歷史
歷史
鋦(Curium)是一種放射性超鈾元素,
符號為Cm,原子序為96,屬於錒系元素,
以研究放射性的科學家瑪麗·居禮(Marie Curie)
和其丈夫皮埃爾·居禮命名。
伯克利加州大學的格倫·西奧多·西博格等人
在1944年7月首次專門合成鋦元素。
發現起初被列為機密,到1945年11月才公佈於世。
大部分的鋦是在核反應爐中通過對鈾或鈽進行中子撞擊產生的。
每噸用盡的核燃料中含有大約
鋦是一種銀白色的堅硬高密度金屬,熔點和沸點是錒系元素中較高的。
鋦在標準溫度和壓力下具順磁性,並在冷卻後變為反鐵磁性; 許多鋦化合物也具有磁性的轉變。
鋦在化合物中的氧化態通常為+3和+4,而在溶液中主要呈+3態。
鋦很容易被氧化,而形成的氧化物是鋦最常見的形態。
鋦可以和各種有機化合物形成螢光配合物,
但不出現在任何細菌或古菌中。當攝入人體之後,鋦會累積在骨骼、肺部和肝臟中,並可致癌。
鋦和鋂在1944年的發現與當時旨在製造原子彈的曼哈頓計劃息息相關。
有關其發現的信息一直保密到1945年才公諸於世。在
美國電台節目「Quiz Kids」(小朋友問答)的一位聽眾問到,戰時除了鎿和鈽之外還又沒有發現其他新的超鈾元素,
格倫·西博格回應時洩露了有關發現鋦和鋂的消息。
鋦是以瑪麗·居禮(Marie Curie)和其丈夫皮埃爾·居禮(Pierre Curie)命名的。
兩人發現了鐳元素,並對放射性作出了相當的貢獻。
這種命名方法參照了元素週期表中位於鋦以上的鑭系元素釓:
釓是以研究稀土元素的科學家、工程師約翰·加多林命名的。
 物理特性
物理特性
α型鋦金屬的雙六方密排晶體結構,層序為ABAC(A:綠色,B:藍色,C:紅)
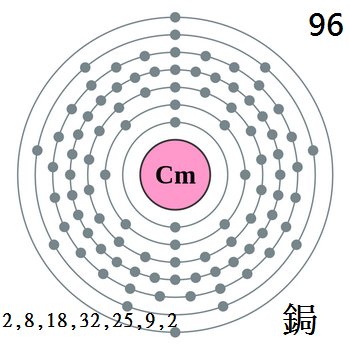
鋦的電子層(2,
8, 18, 32, 25, 9, 2)
三(氫三)吡唑基硼酸根鋦(III)配合物中Cm3+離子經波長為396.6
nm的光照射後,發出橙色的螢光。
鋦是一種放射性人工合成元素,也是質地堅硬、密度高的銀白色金屬。其物理和化學特性與釓相似。
鋦的熔點為
而釓的熔點則在
鋦的磁特性奇特。其旁邊的錒元素在不同溫度下都不會偏離居禮外斯順磁性,
但α鋦會在冷卻至65至52
K時轉變為反鐵磁性,而β鋦在大約205
K時轉變成亞鐵磁性。
另外,鋦和氮族元素的化合物在冷卻後會轉成鐵磁性:
鋦的鑭系同系物釓以及釓的氮族元素化合物也會在冷卻時轉變磁性,
但稍有不同:Gd和GdN變為鐵磁性,而GdP、GdAs和GdSb則具反鐵磁性。
鋦的電阻率會隨溫度而變化:在4至60 K時大約翻倍,並從60 K到室溫幾乎保持恆等。
鋦的電阻率與釓、鈽和鎿相近,但比鋂、鈾、釙和釷高出許多。
化學特性
鋦的最穩定氧化態為+3,其離子在溶液中也具有+3態。
其+4態只出現在少有的幾個固態化合物中,如CmO2和CmF4。
鋦的化學特性與同為錒系元素的釷和鈾不同,但和鋂及許多鑭系元素相似。
在水溶液中,Cm3+離子可以是無色或淺綠色的,而Cm4+離子則是淺黃色的。
Cm3+的吸收光譜在375.4、381.2和396.5奈米波長處有尖銳的峰值,
這些峰值的強度可以直接用來測量該離子的濃度。
鋦離子屬於硬酸,因此可以和硬鹼產生最穩定的配合物。
合成
同位素的製備
鋦是在核反應爐中少量產生的。到目前為止,
其餘更重的同位素只有數克或甚至數毫克的總產量。
故此鋦的價格昂貴,每毫克160至185美元;更近期的估價為:
在反應爐中,238U可以通過一系列的核反應形成鋦。
首先238U捕獲一顆中子,變為239U,再經β–衰變形成239Np和239Pu。
實際研究在製造鋦的時候,並不對鈾進行照射,而是用鈽。
乏核燃料中含有大量的鈽,能夠輕易地提取使用。
如果使用高中子通量的輻射,能通過另一條反應鏈形成
鋦金屬的製備
層析洗提曲線,能看出鑭系的鋱(Tb)、釓(Gd)和銪(Eu)與相應錒系的錇(Bk)、鋦(Cm)和鋂(Am)之間的相近之處。
一般的合成產物含有不同鋦同位素的氧化物混合物。
要分離出其中一種同位素,可以將乏核燃料(如混合氧化物核燃料)溶於硝酸中,
再使用磷酸三丁酯和烴類的混合物,通過鈾鈽分離(PUREX)來萃取出大部分的鈾和鈽。
然後利用二醯胺來萃取水溶殘餘物(殘液)中剩餘的鑭系元素和錒系元素。
產物將會是三價錒系及鑭系元素的混合物。要分離出當中的鋦化合物,可用多重步驟的層析法及離心法,並使用適當的試劑。
其中一種可用來專門提取鋦的試劑為雙三嗪基二吡啶配合物。
科學家通過對鋦化合物進行還原反應來取得處於金屬態的鋦元素。
其中一種可用於製備鋦金屬的化合物為三氟化鋦。
反應必須在不含水或氧的環境下進行,使用鉭和鎢造的器具,並以鋇或鋰作為還原劑。
另一可行方法是在氯化鎂和氟化鎂的熔化混合物中用鎂鋅合金來還原二氧化鋦。